Đề cương ôn tập giữa học kì 1 môn Hóa học 10 sách Kết nối tri thức với cuộc sống Ôn tập giữa kì 1 môn Hóa 10
Đề cương ôn tập giữa kì 1 Hóa học 10 Kết nối tri thức năm 2024 - 2025 bao gồm giới hạn ôn tập và một số câu hỏi trắc nghiệm kết hợp tự luận. Nội dung ôn tập giữa kì 1 Hoạt động trải nghiệm 10 được biên tập một cách logic và khoa học có đáp án kèm theo. Qua đó giúp các em học sinh lớp 10 nắm được kiến thức mình đã học trong chương trình giữa kì 1, rèn luyện và ôn tập một cách hiệu quả.
Đề cương giữa kì 1 Hóa học 10 Kết nối tri thức còn giúp giáo viên khái quát được nội dung ôn tập và nâng cao được hiệu quả ôn tập cho học sinh, tránh được tình trạng ôn tập cục bộ hoặc tràn lan. Vậy dưới đây là toàn bộ đề cương ôn tập Hóa học 10 giữa kì 1 Kết nối tri thức mời các bạn cùng theo dõi nhé.
Đề cương ôn tập giữa kì 1 Hóa học 10 Kết nối tri thức
CHƯƠNG I – CẤU TẠO NGUYÊN TỬ
A. TÓM TẮT LÝTHUYẾT:
1. Thành phần nguyên tử
Nguyên tử là hạt trung hòa về điện, có cấu tạo 2 phần:
+ Nhân nguyên tử: proton (p) mang điện dương, neutron (n) không mang điện.
+ Vỏ nguyên tử: các electron (e) mang điện âm.
Khối lượng nguyên tử coi như bằng khối lượng hạt nhân (khối lượng các hạt proton và neutron).
|
Cấu tạo nguyên tử |
Vỏ nguyên tử |
Hạt nhân |
|
|
Electron |
Proton |
Neutron |
|
|
Điện tích |
1- |
1+ |
0 |
|
Khối lượng (amu) |
0,00055 |
1 |
1 |
Số Avorgaro: Số nguyên tử hay phân tử có trong 1 mol chất luôn bằng6,023.1023.
Đơn vị đo khối lượng nguyên tử: 1amu = 1 khối lượng Cacbon ≈1,6605.10-27
2. Hạt nhân nguyên tử
Ký hiệu Z cho biết:
+ Số proton trong hạt nhân.
+ Số electron trong lớp vỏ.
+ Điện tích hạt nhân là: Z+.
+ Số đơn vị điện tích hạt nhân: Z.
+ Số hiệu nguyên tử.
Số khối: A = Z +N
............
II. Bài tập tự luận:
Bài 1: Cho các nguyên tử có kí hiệu sau:
![]()
a. Có bao nhiêu nguyên tố hóa học?
b. Những nguyên tử nào là đồng vị của nhau?
c. Những nguyên tử nào cùng số khối?
d. Những nguyên tử nào cùng số neutron?
e. Viết cấu hình e của các nguyên tử trên?
f. Các nguyên tử trên là kim loại, phi kim hay khí hiếm?
g. Xác định số e độc thân trong mỗi nguyên tử trên?
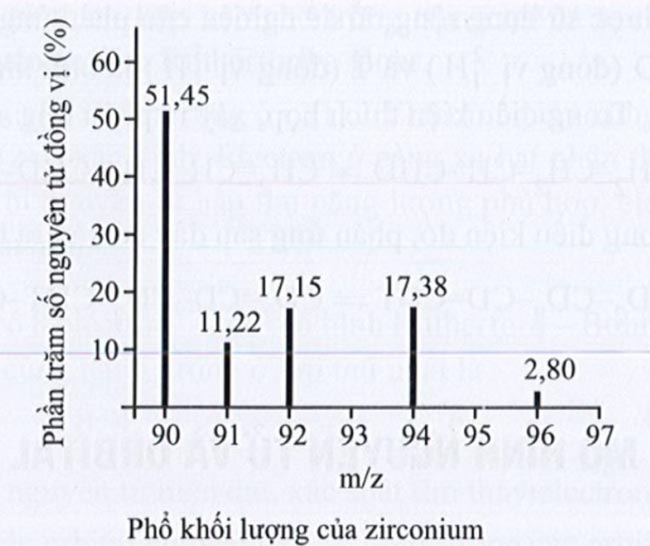
Bài 2: Phổ khối lượng của zirconium (Zr) được biểu diễn như hình sau đây (điện tích z của các đồng vị Zr đều bằng 1+). Hãy xác định số lượng đồng vị bền và tính nguyên tử khối trung bình của Zr?
Bài 3: Trong thể dục thể thao, có một số vận động viên sử dụng các loại chất kích thích trong thi đấu – gọi là doping, dẫn đến thành tích đạt được của họ không thật so với năng lực vốn có. Một trong các loại doping thường gặp là testosterone tổng hợp.
Tỉ lệ giữa 2 đồng vị C-12 (98,89 %) và C-13 (1,11%) là không đổi đối với testossterone tự nhiên trong cơ thể. Trong khi testosterone tổng hợp có phần trăm C-13 ít hơn testossterone tự nhiên. Đây chính là mấu chốt của xét nghiệm CIR – (carbon isotope ratio – tỉ lệ đồng vị carbon) – một xét nghiệm với mục đích xác định xem vận động viên có sử dụng doping hay không.
Giả sử thực hiện phân tích CIR với một vận động viện thu được kết quả % số nguyên tử C-12 là x, C-13 là
Từ tỉ lệ này tính được NTK trung bình của carbon trong mẫu phân tích là 12,0098. Với kết quả thu được em có nghi ngờ vận động viên này sử dụng doping không? Vì sao?
Bài 4: Trong tự nhiên, copper (đồng) có 2 đồng vị 63Cu và ACu, trong đó đồng vị 65Cu chiếm 27% về số nguyên tử. Nguyên tử khối trung bình của copper là 63,54.
Tính A?
Tính phần trăm khối lượng của 63Cu trong kim loại đồng tựnhiên?
Tính phần trăm khối lượng của 63Cu trong CuSO4 (cho O = 16, S =32)?
Bài 5: Một nguyên tố X chủ yếu gồm hai đồng vị bền là X1 và X2. Đồng vị X1 có tổng số hạt là 18. Đồng vị X2 có số hạt mang điện nhiều hơn số hạt không mang điện là 5. Nguyên tử khối trung bình của X là 12,011. Xác định phần trăm số nguyên tử của các đồng vị X1, X2?
Bài 6*: Hợp chất có công thức phân tử M2X được ứng dụng trong sản xuất xi măng, phân bón, hàm lượng
% khối lượng M2X được dùng để đánh giá độ dinh dưỡng của phân lân…. Biết phân tử M2X có tổng số hạt là 140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của nguyên tử M nhiều hơn số khối của nguyên tử X là 23. Tổng số hạt trong nguyên tử M nhiều hơn trong nguyên tử X là 34. Hãy viết cấu hình e của nguyên tử M, X, ion M+, X2-. Xác định tính chất KL hay PK và số e độc thân trên từng nguyên tử M, X?
..........
III. Bài tập trắc nghiệm
I. Câu hỏi trắc nghiệm:
Thành phần nguyên tử - Nguyên tố hóa học – Đồng vị
Câu 1: Nguyên tố hoá học là
A. những nguyên tử có cùng số neutron.
B. những nguyên tử có cùng điện tích hạt nhân.
C. những phân tử có cùng phân tử khối.
D. những nguyên tử có cùng số khối.
Câu 2: Cho các phát biểu sau
(1). Tất cả các hạt nhân nguyên tử đều được cấu tạo từ các hạt proton và neutron. (2). Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ.
(3). Trong nguyên tử số electron bằng số proton.
(4). Trong hạt nhân, nguyên tử hạt mang điện là proton và electron.
(5). Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại. Số phát biểu đúng là
A. 1
B. 2
C. 3
D. 4
Câu 3: Cho nguyên tử X có tổng số hạt là 34, trong đó số hạt mang điện gấp 1,8333 lần số hạt không mang điện. Xác định số khối X?
........
Tải file tài liệu để xem thêm Đề cương ôn tập giữa kì 1 Hóa học 10 Kết nối tri thức
Chọn file cần tải:
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây:












 Toán 10 Kết nối tri thức
Toán 10 Kết nối tri thức
 Toán 10 Chân trời sáng tạo
Toán 10 Chân trời sáng tạo
 Toán 10 Cánh Diều
Toán 10 Cánh Diều
 Soạn văn 10 Chân trời sáng tạo
Soạn văn 10 Chân trời sáng tạo
 Soạn văn 10 Cánh Diều
Soạn văn 10 Cánh Diều
 Soạn văn 10 Kết nối tri thức
Soạn văn 10 Kết nối tri thức
 Tiếng Anh 10 Global Success
Tiếng Anh 10 Global Success
 Tiếng anh 10 Friends Global
Tiếng anh 10 Friends Global
 Tiếng Anh 10 Explore New Worlds
Tiếng Anh 10 Explore New Worlds









