| |
KHTN 8: Bài tập Chủ đề 2 Giải KHTN 8 Cánh diều trang 72
Bài trước
Giải bài tập KHTN 8 Bài tập Chủ đề 2 giúp các em học sinh trả lời các câu hỏi trong SGK Khoa học tự nhiên 8 Cánh diều trang 72.
Giải Khoa học tự nhiên 8 Bài tập Chủ đề 2 được biên soạn bám sát theo chương trình SGK. Đồng thời, cũng giúp thầy cô tham khảo để soạn giáo án Bài tập Chủ đề 2: Acid - Base - pH - Oxide - Muối - Phần 1: Chất và sự biến đổi chất cho học sinh của mình. Vậy mời thầy cô và các em cùng theo dõi nội dung chi tiết trong bài viết dưới đây của Eballsviet.com:
Câu 1
Trong các chất sau, chất nào là acid, base, kiềm?
HCl, CuO, KOH, CaCO3, H2SO4, Fe(OH)22.
Trả lời:
Chất là acid: HCl, H2SO4.
Chất là base: KOH, Fe(OH)2.
Chất là kiềm: KOH.
Câu 2
Trong các chất sau, chất nào là muối, oxide base, oxide acid: CuSO4, SO2, MgCl2, CaO, Na2CO3. Viết tên gọi các muối.
Trả lời:
- Chất là muối: CuSO4; MgCl2; Na2CO3.
Tên gọi các muối:
- CuSO4: copper(II) sulfate.
- MgCl2: magnesium chloride.
- Na2CO3: sodium carbonate.
- Chất là oxide base: CaO.
- Chất là oxide acid: SO2.
Câu 3
Chất nào trong dãy chất sau: CuO, Mg(OH)2, Fe, SO2, HCl, CuSO4 tác dụng được với:
a) dung dịch NaOH.
b) dung dịch H2SO4loãng.
Viết phương trình hóa học của các phản ứng (nếu có).
Trả lời:
a) Các chất tác dụng được với dung dịch NaOH là: SO2, HCl, CuSO4.
Phương trình hóa học minh họa:
SO2 + 2NaOH → Na2SO3 + H2O
HCl + NaOH → NaCl + H2O
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
b) Các chất tác dụng được với dung dịch H2SO4loãng là: CuO, Mg(OH)2, Fe.
Phương trình hóa học minh họa:
CuO + H2SO4 → CuSO4 + H2O
Mg(OH)2 + H2SO4 → MgSO4 + 2H2O
Fe + H2SO4 (loãng) → FeSO4 + H2↑.
Câu 4
Viết các phương trình hoá học theo các sơ đồ sau:
a) HCl + ? − − − → NaCl + H2O
b) NaOH + ? − − − → Cu(OH)2↓ + ?
c) KOH + ? − − − → K2SO4+ ?
d) Ba(NO3)2+ ? − − − → BaSO4↓ + ?
Trả lời:
a) HCl + NaOH → NaCl + H2O
b) 2NaOH + CuCl2→ Cu(OH)2↓ + 2NaCl
c) 2KOH + CuSO4→ K2SO4+ Cu(OH)2↓
d) Ba(NO3)2+ Na2SO4→ BaSO4↓ + 2NaNO3.
Câu 5
Viết các phương trình hóa học theo các sơ đồ chuyển hóa sau:
![]() \(a) CuO \overset{+ ?}{\rightarrow} CuSO4 \overset{+ ?}{\rightarrow} Cu(OH)2\)
\(a) CuO \overset{+ ?}{\rightarrow} CuSO4 \overset{+ ?}{\rightarrow} Cu(OH)2\)
![]() \(b) Mg \overset{+ ?}{\rightarrow} MgCl2 \overset{+ ?}{\rightarrow} Mg(OH)2\)
\(b) Mg \overset{+ ?}{\rightarrow} MgCl2 \overset{+ ?}{\rightarrow} Mg(OH)2\)
![]() \(c) NaOH \overset{+ ?}{\rightarrow} Na2SO4 \overset{+ ?}{\rightarrow} NaCl\)
\(c) NaOH \overset{+ ?}{\rightarrow} Na2SO4 \overset{+ ?}{\rightarrow} NaCl\)
![]() \(d) K2CO3 \overset{+ ?}{\rightarrow} CaCO3 \overset{+ ?}{\rightarrow} CaCl2\)
\(d) K2CO3 \overset{+ ?}{\rightarrow} CaCO3 \overset{+ ?}{\rightarrow} CaCl2\)
Trả lời:
a) CuO + H2SO4 → CuSO4 + H2O
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
b) Mg + 2HCl → MgCl2 + H2↑
MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl.
c) 2NaOH + H2SO4 → Na2SO4 + 2H2O
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓.
d) K2CO3 + CaCl2 → CaCO3↓ + 2KCl
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O.
Câu 6
Cho 100 mL dung dịch Na2SO4 0,5 M tác dụng vừa đủ với dung dịch BaCl2 thì thu được m gam kết tủa.
a) Viết phương trình hoá học của phản ứng xảy ra.
b) Tính m.
c) Tính nồng độ mol của dung dịch BaCl2, biết thể tích dung dịch BaCl2 đã dùng là 50 mL.
Trả lời:
a) Phương trình hóa học của phản ứng xảy ra:
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl
b) Đổi 100 mL = 0,1 lít.
Theo bài ra: nNa2SO4 = 0,1 × 0,5 = 0,05 (mol)
Theo phương trình hóa học: nBaSO4 = nNa2SO4 = 0,05 (mol) .
Vậy m = 0,05 × (137 + 32 + 16 × 4) = 11,65 (gam).
c) Theo phương trình hoá học: nBaCl2 = nNa2SO4 = 0,05 (mol) .
Đổi 50 mL = 0,05 lít.
Nồng độ mol của dung dịch BaCl2 là:
![]() \(C_M=\frac{n}{V}=\frac{0,05}{0,05}=1M\)
\(C_M=\frac{n}{V}=\frac{0,05}{0,05}=1M\)
Câu 7
Viết các phương trình hoá học điều chế MgCl2 trực tiếp từ NgO, Mg(OH)2, MgSO4.
Trả lời:
Các phương trình hóa học:
MgO + 2HCl → MgCl2 + H2O
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
MgSO4 + BaCl2 → MgCl2 + BaSO4 ↓.
Câu 8
Biết dung dịch NaCl có pH bằng 7. Chỉ dùng quỳ tím, nêu cách nhận biết các dung dịch không màu, đựng trong ba ống nghiệm riêng rẽ: NaOH, HCl và NaCl.
Câu 9
Việc bón phân NPK cho cây cà phê sau khi trồng bốn năm được chia thành bốn thời kì như sau:
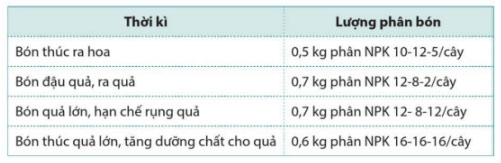
a) Tính lượng N đã cung cấp cho cây trong cả bốn thời kì.
b) Nguyên tố dinh dưỡng potassium được bổ sung cho cây nhiều nhất ở thời kì nào?
Liên kết tải về
KHTN 8: Bài tập Chủ đề 2
243,2 KB
Tải về
Xác thực tài khoản!
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây:
Số điện thoại chưa đúng định dạng!
Sắp xếp theo
Chủ đề liên quan
Tìm bài trong mục này
Đóng
Chỉ thành viên Download Pro tải được nội dung này!
Download Pro - Tải nhanh, website không quảng cáo!
Tìm hiểu thêm












 Toán 8 Kết nối tri thức
Toán 8 Kết nối tri thức
 Toán 8 Cánh Diều
Toán 8 Cánh Diều
 Toán 8 Chân trời sáng tạo
Toán 8 Chân trời sáng tạo
 Toán 8
Toán 8
 Soạn Văn 8 Kết nối tri thức
Soạn Văn 8 Kết nối tri thức
 Soạn văn 8 Chân trời sáng tạo
Soạn văn 8 Chân trời sáng tạo
 Soạn Văn 8 Cánh Diều
Soạn Văn 8 Cánh Diều
 Chuyên đề Ngữ văn 8
Chuyên đề Ngữ văn 8
 Văn mẫu 8 Kết nối tri thức
Văn mẫu 8 Kết nối tri thức
 Văn mẫu 8 Chân trời sáng tạo
Văn mẫu 8 Chân trời sáng tạo








